Átomos Estáveis com Massa Atômica Superior a 83: Exemplo De Atomos Estaveis Com Massa Atomica Maior Que 83
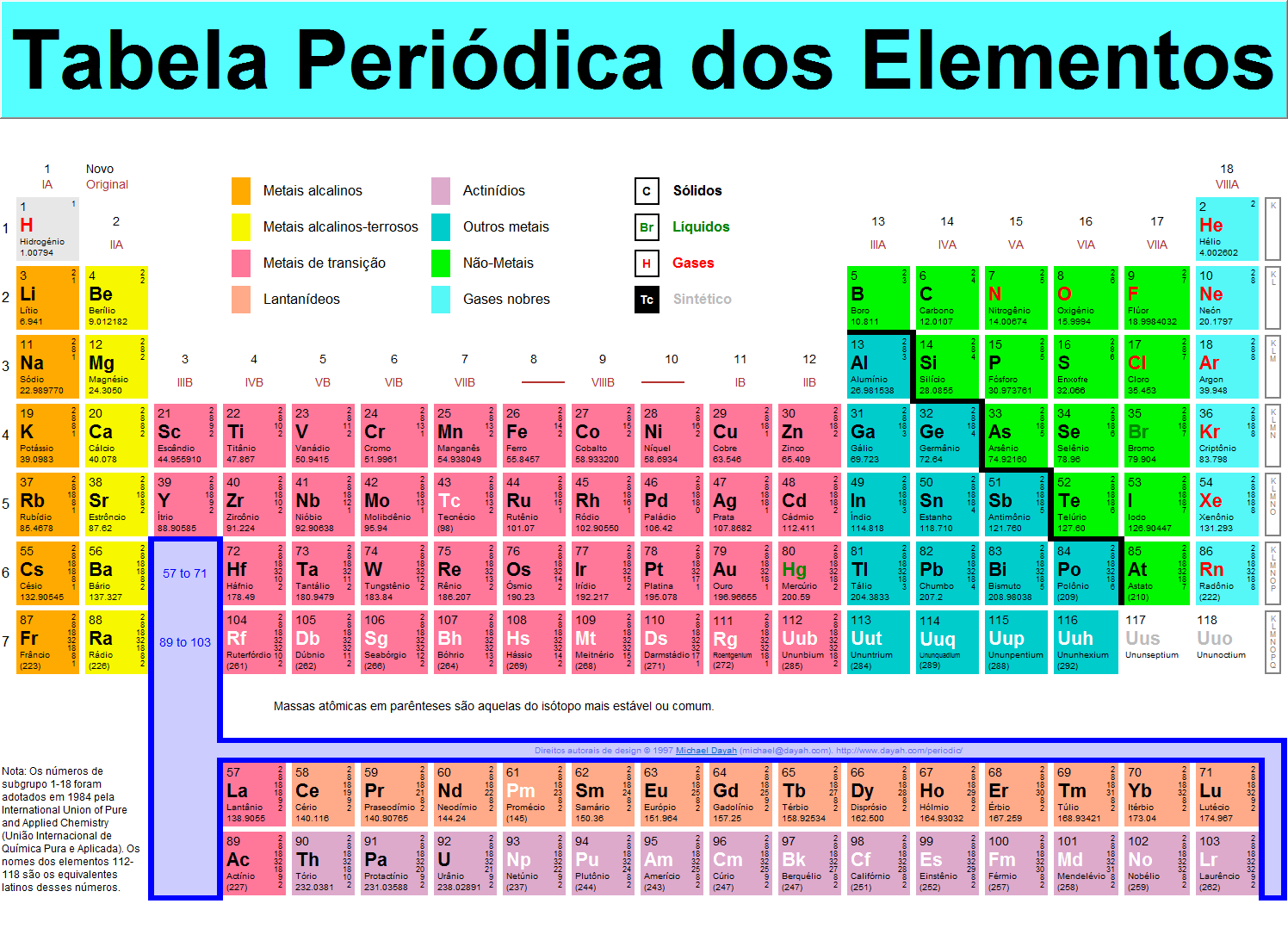
Exemplo De Atomos Estaveis Com Massa Atomica Maior Que 83 – A estabilidade nuclear é um fenômeno complexo que depende da interação entre as forças nucleares fortes e fracas, bem como da razão entre o número de prótons e nêutrons no núcleo atômico. Átomos com massa atômica superior a 83 geralmente apresentam maior instabilidade devido ao aumento da repulsão eletrostática entre os prótons. No entanto, alguns isótopos com massas atômicas elevadas conseguem alcançar estabilidade, um aspecto crucial na compreensão da estrutura da matéria e com importantes aplicações em diversas áreas.
Estabilidade Nuclear e Massa Atômica
O número atômico (Z) representa a quantidade de prótons no núcleo de um átomo, definindo o elemento químico. O número de massa (A) é a soma do número de prótons e nêutrons. A estabilidade nuclear está intrinsecamente ligada à razão próton-nêutron (N/Z). Para átomos leves, uma razão próxima a 1 indica maior estabilidade. Conforme a massa atômica aumenta, a razão ideal para estabilidade se desvia de 1, necessitando de um maior número de nêutrons para contrabalançar a repulsão eletrostática entre os prótons.
Números mágicos de prótons e nêutrons (2, 8, 20, 28, 50, 82, 126) também contribuem significativamente para a estabilidade nuclear, pois correspondem a camadas nucleares completamente preenchidas, conferindo maior estabilidade ao núcleo.
Exemplos de Isótopos Estáveis com Massa Atômica > 83
Apesar da tendência à instabilidade em átomos pesados, alguns isótopos apresentam estabilidade nuclear. A seguir, uma tabela com exemplos:
| Símbolo | Número Atômico (Z) | Massa Atômica (A) | Abundância Natural (%) |
|---|---|---|---|
| 192Pt | 78 | 192 | 0.78 |
| 194Pt | 78 | 194 | 32.97 |
| 195Pt | 78 | 195 | 33.83 |
| 196Pt | 78 | 196 | 25.24 |
| 198Pt | 78 | 198 | 7.16 |
| 202Hg | 80 | 202 | 29.86 |
| 204Hg | 80 | 204 | 6.85 |
| 208Pb | 82 | 208 | 52.4 |
| 180Ta | 73 | 180 | 0.012 |
| 180Hf | 72 | 180 | 0.35 |
Os isótopos de platina (Pt), mercúrio (Hg) e chumbo (Pb) listados acima são encontrados na natureza em diversas concentrações. O chumbo-208, por exemplo, é o isótopo mais abundante do chumbo. As aplicações desses isótopos variam. A platina é usada em joias e catalisadores industriais; o mercúrio, apesar de sua toxicidade, tem aplicações em termômetros e lâmpadas; o chumbo é usado em baterias e proteção contra radiação.
As propriedades químicas desses isótopos são semelhantes, uma vez que são isótopos do mesmo elemento, mas suas propriedades físicas, como densidade e ponto de fusão, podem variar ligeiramente.
Forças Nucleares e Estabilidade
A estabilidade nuclear de átomos pesados é governada pelas forças nucleares fortes e fracas. A força nuclear forte atrai prótons e nêutrons, superando a repulsão eletrostática entre os prótons. A força nuclear fraca é responsável pelo decaimento beta, um processo que converte um nêutron em um próton (ou vice-versa), alterando a razão N/Z. A energia de ligação nuclear representa a energia necessária para separar os núcleons (prótons e nêutrons) do núcleo.
Quanto maior a energia de ligação por núcleon, maior a estabilidade do núcleo. Isótopos instáveis com massa atômica acima de 83 geralmente sofrem decaimento radioativo, como decaimento alfa (emissão de uma partícula alfa, 4He), decaimento beta (emissão de um elétron ou pósitron) ou decaimento gama (emissão de um fóton de alta energia).
Isótopos Estáveis e Instáveis Próximos à Massa Atômica 83, Exemplo De Atomos Estaveis Com Massa Atomica Maior Que 83
A estabilidade nuclear varia significativamente ao redor da massa atômica 83. Isótopos com massa atômica ligeiramente abaixo de 83 tendem a ser mais estáveis do que aqueles imediatamente acima. Há uma tendência de aumento da instabilidade à medida que a massa atômica aumenta além de 83, devido ao aumento da repulsão coulombiana entre os prótons. Observa-se uma região de relativa instabilidade nessa região, com muitos isótopos sofrendo decaimento radioativo.
Um gráfico mostrando a relação entre a massa atômica e a estabilidade nuclear para isótopos próximos a 83 mostraria um pico de estabilidade próximo a 83 (mas ligeiramente abaixo), seguido por uma queda na estabilidade à medida que a massa atômica aumenta. O gráfico apresentaria pontos discretos representando os isótopos, com os isótopos estáveis representados por pontos mais altos no eixo vertical (representando estabilidade) e os isótopos instáveis por pontos mais baixos, com a altura do ponto refletindo a meia-vida do isótopo (isótopos com meias-vidas mais curtas teriam pontos mais baixos).
Aplicações de Isótopos Estáveis com Massa Atômica > 83
Isótopos estáveis com massa atômica superior a 83 encontram aplicações em diversas áreas. Por exemplo, isótopos de platina são usados como catalisadores em reações químicas industriais, explorando sua capacidade de acelerar reações sem serem consumidos. Isótopos de chumbo são usados em aplicações de blindagem contra radiação devido à sua alta densidade e capacidade de absorver partículas radioativas. Em pesquisa científica, esses isótopos podem ser usados como traçadores em estudos de reações químicas e processos biológicos, permitindo o monitoramento de compostos específicos.
O estudo desses isótopos é fundamental para o avanço científico e tecnológico, pois contribui para uma melhor compreensão da estrutura nuclear, dos processos de decaimento radioativo e das propriedades físico-químicas dos elementos. Este conhecimento impulsiona o desenvolvimento de novas tecnologias em áreas como medicina nuclear, produção de energia e ciência de materiais.
Quais são as implicações da descoberta de isótopos estáveis com massa atômica acima de 83?
A descoberta desafia os modelos teóricos de estabilidade nuclear, impulsionando pesquisas para aprimorá-los e entender melhor as forças nucleares. Além disso, abre novas possibilidades para aplicações em diversas áreas, como a medicina e a indústria.
Existe algum limite superior para a massa atômica de um isótopo estável?
Embora isótopos estáveis acima de 83 sejam raros, não há um limite superior definido teoricamente. A estabilidade depende de um complexo equilíbrio de forças nucleares e a probabilidade de encontrar isótopos estáveis com massas atômicas extremamente elevadas diminui significativamente.
Como a abundância natural desses isótopos influencia suas aplicações?
A baixa abundância natural de muitos desses isótopos pode limitar suas aplicações, necessitando de métodos de enriquecimento isotópico. No entanto, mesmo em baixas concentrações, suas propriedades únicas podem ser exploradas em aplicações específicas.

